α-螺旋
的有关信息介绍如下: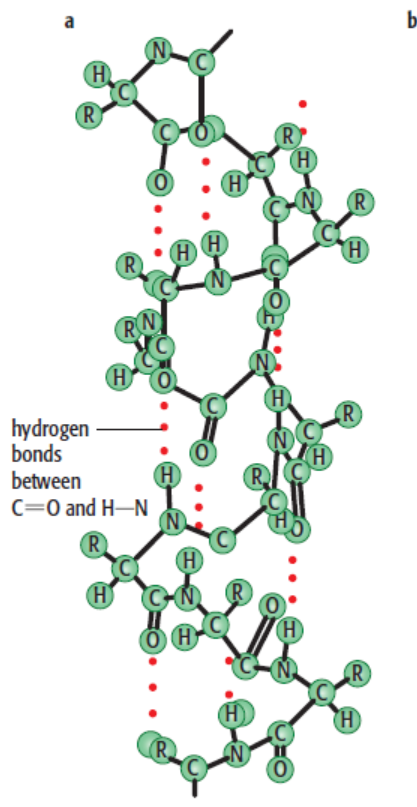
α-螺旋(α-helix)是蛋白质二级结构的主要形式之一。指多肽链主链围绕中心轴呈有规律的螺旋式上升,每3.6 个氨基酸残基螺旋上升一圈,向上平移0.54nm,故螺距为0.54nm,两个氨基酸残基之间的距离为0.15nm。螺旋的方向为右手螺旋。氨基酸侧链R基团伸向螺旋外侧,每个肽链的肽键的羰基氧和第四个N-H形成氢键,氢键的方向与螺旋长轴基本平行。由于肽链中的全部肽键都可形成氢键,故α-螺旋十分稳定。
想要了解更多“α-螺旋”的信息,请点击:α-螺旋百科

α-螺旋(α-helix)是蛋白质二级结构的主要形式之一。指多肽链主链围绕中心轴呈有规律的螺旋式上升,每3.6 个氨基酸残基螺旋上升一圈,向上平移0.54nm,故螺距为0.54nm,两个氨基酸残基之间的距离为0.15nm。螺旋的方向为右手螺旋。氨基酸侧链R基团伸向螺旋外侧,每个肽链的肽键的羰基氧和第四个N-H形成氢键,氢键的方向与螺旋长轴基本平行。由于肽链中的全部肽键都可形成氢键,故α-螺旋十分稳定。
想要了解更多“α-螺旋”的信息,请点击:α-螺旋百科